Origine de l’arsenic (As):
L’arsenic n’est pas un élément trouvé naturellement dans l’eau comme le sodium ou le calcium. Il est introduit dans l’eau par les activités activités minières, la métallurgie, l’agriculture (l’engrais è base de phosphate peut contenir de l’arsenic) et d’autres activités industrielles. L’As est très toxique. C’est un contaminant réglementé dans différentes législations dont le Québec ou sa concentration maximale admissible est de 50 microgramme par litre.
Chimie de l’arsenic dans l’eau
L’arsenic pur n’est pas soluble dans l’eau, mais la plupart de ses composés le sont.
L’arsenic (masse atomique 74,92), configuration électronique 1s2 2s2 2p6 3s2 3p6 3d104s24p3 est susceptible de perdre ses électons (les 3 électron p puis les 2 électrons s). Ainsi les états d’oxydation principaux sont 3 (As3+) et 5 (As5+). Mais il peut aussi existes les états 2,1 et -3.
Dans l’eau, l’arsenic a deux états d’oxydation prépondérants (III et V), mais il n’est pas sous forme cationique libre. Il est plutôt sous forme:
d’arsenite (As (III)), état d’oxydation 3, représenté par la structure H3AsO3. (H3AsO3/H2AsO3, pKa = 9,2)
d’arsenate (As(V), état d’oxydation 5, représenté par H3AsO4. (H3AsO4/H2AsO4, pKa = 2,7; H2AsO4/HAsO4, pKa = 6,8; HAsO4/AsO4, pKa = 11,5.
Selon les pKa des composés présentés, on retrouve aux pH des eaux naturels une concentration nettement plus importante d’arsenites que d’arsenate.
Nomination des espèces:
H2AsO4- : ion dihydrogénoarséniate.
HAsO42- : ion hydrogénoarséniate.
AsO43- : ion arséniate.
H2AsO3- : acide dihydrogénoortho-arsénite.
HAsO32- : acide hydrogénoortho-arsénite.
AsO33- : ion arsénite.
Aux pH des eaux naturelles (entre 6 et 9), on retrouve l’arsenite neutre (H3AsO3) en forte proportion et les espèces H2AsO4(-) et HAsO4(2-).
Toutes les espèces de l’arsenic dans l’eau naturelle sont à l’état neutre ou chargées négativement, et cela aura une influence sur le type de traitement.
Traitements de l’arsenic
Les techniques permettant de traiter partiellement ou efficacement l’arsenic dans l’eau sont:
Coprécipitation / filtration (avec sels de fer, alun, chaux, …)
Osmose inverse – Nanofiltration après oxydation
Alumine activée
Oxydation filtration fine
Échange ionique (résine anionique)
Distillation (98% +)
Sable vert (presence d’une certaine concentration de fer)
De tous les traitements, l’osmose inverse est la seule technologie qui enlève l’As aux plus fortes proportions qu’il soit à l’état d’arsenite ou d’arsenate
Coprécipitation ou coagulation suivie de la filtration
La coprécipitation peut se faire avec le fer (FeCl3), l’alun ou la chaux. Quelque soit le réactif, il est moins efficace lorsque l’arsenic est sous forme d’arsenite (<50%) et . Le taux d’enlèvement est inférieur à 40% lorsqu’il est sous forme d’arsenate, le taux d’elèvement est au-dela de 80%.
Généralement le chlorure de fer (FeCl3) est utilisé. Le fer précipite avec l’arsenate (FeAsO4) et les particules formées de taille autour de 50 microns seront filtrés. Les chlorures permettent sumultanément d’oxyder l’arsenite en Arsenate, ce qui permet d’avoir des résultats intéressants.
Osmose inverse
Permet l’enlèvement 95 à 100% de L’arsenate, mais pour l’arsenite, le taux d’enlèvement est entre 60 et 80%. L’enlèvement typique de l’arsenic dans l’eau par une membrane d’osmose varie typiquement entre 80 et 97%.
La nanofiltration est efficace pour l’enlèvement de l’arsenate (60-80%) mais très très peu pour l’arsenite (moins de 30%). Une oxydation de l’arsenic est nécessaire avant la nanofiltration.
Alumine activée
Peut enlever l’arsenate efficacement à pH entre 5.5 et 6, mais inefficace pour le traitement de l’arsenite. L’efficacité est réduite pour par la présence d’autres anions comme les sulfates.
Résine anionique
Elle peut être efficace dépendamment des autres ions en présence et des fraction ionique vs anionique.
Les résines anioniques fortes ont une grande sélectivité pour l’arsenate, mais un faible sélectivité pour l’arsenite. Ces résines ont même moins de sélectivité pour l’arsenate que les sulfates. Ainsi s’il y a beaucoup de sulfate, le procédé n’est pas viable, car le sulfate va déloger l’arsenic et on pourrait avoir une concentration d’arsenic plus importante à l’effluent.
Certaines compagnies ont développé des résines spécifiques (ex Resintech ASM-10-HP) mais elles sont toutes moins efficaces lorsque l’arsenic est sous forme d’arsenite.
Diagramme Potentiel-pH Arsenic
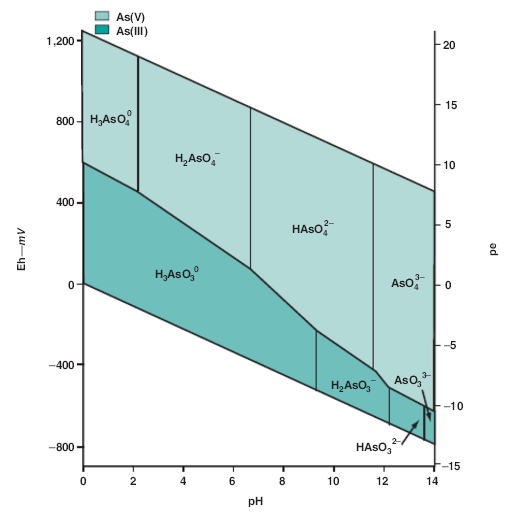
Adapté de : Kenneth W. Moore
RÉFÉRENCES:
David B. Vance
Kenneth W. Moore
Resintech ASM-10-HP
 Mon Agora – Blog La parole est à moi
Mon Agora – Blog La parole est à moi
